|
تضامنًا مع حق الشعب الفلسطيني |
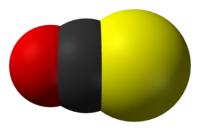
كبريتيد الكربونيل
| كبريتيد الكربونيل | |
|---|---|
| الاسم النظامي (IUPAC) | |
| الخواص | |
| الصيغة الجزيئية | COS |
| الكتلة المولية | 60.07 غ/مول |
| المظهر | غاز عديم اللون |
| الكثافة | 2.72 غ/ل |
| نقطة الانصهار | -139 °س |
| نقطة الغليان | − 50 °س |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
كبريتيد الكربونيل (أو سلفيد الكربونيل) هو مركب كيميائي يتألف من عناصر الكبريت والكربون والأكسجين، صيغته COS، ويوجد على شكل غاز عديم اللون، وهو من المركبات السامة.
الوفرة والتحضير
يوجد غاز كبريتيد الكربونيل بكميات نزرة في الغلاف الجوي للأرض، حيث ينطلق من البراكين والمنافس الحرارية المائية في المحيطات.
يحضر المركب مخبرياً من تفاعل ثيوسيانات البوتاسيوم مع حمض الكبريتيك حيث تتشكل منتجات ثانوية من بيكبريتات البوتاسيوم وبيكبريتات الأمونيوم:[2]
الخواص
يوجد المركب في الشروط القياسية على شكل غاز عديم اللون، وهو يتألف بنيوياً من ذرة كربون مركزية ترتبط برابطتين ثنائيتين على طرفيها مع الكبريت والأكسجين.
يعطي كبريتيد الكربونيل عند أكسدته في الهواء غازي ثنائي أكسيد الكربون وثنائي أكسيد الكبريت:
كما يتفاعل مع الماء بتفاعل حلمهة (تحلل مائي) ليعطي كبريتيد الهيدروجين بالإضافة إلى ثنائي أكسيد الكربون:[3][4][5]
الدور الحيوي
يعتقد أن لهذا المركب دوراً في تطور نشوء الحياة.[6]
مراجع
- ^ أ ب International Union of Pure and Applied Chemistry (2005). Nomenclature of Inorganic Chemistry (IUPAC Recommendations 2005). Cambridge (UK): Royal Society of Chemistry–International Union of Pure and Applied Chemistry (IUPAC). (ردمك 0-85404-438-8). p. 292. نسخة إلكترونية باللغة الإنجليزية.
- ^ P. D. N. Svoronos, T. J. Bruno: Carbonyl Sulfide: A Review of Its Chemistry and Properties. In: Ind. Eng. Chem. Res. 41, 2002, S. 5321–5336, doi:10.1021/ie020365n.
- ^ "Carbonyl Sulfide CASRN: 463-58-1". Hazardous Substances Data Bank. National Library of Medicine. مؤرشف من الأصل في 2020-02-29.
- ^ "Chemical Summary for Carbonyl Sulfide". U.S. Environmental Protection Agency. مؤرشف من الأصل في 2015-09-24.
- ^ Protoschill-Krebs، G.؛ Wilhelm، C.؛ Kesselmeier، J. (1996). "Consumption of carbonyl sulphide (COS) by higher plant carbonic anhydrase (CA)". Atmospheric Environment. ج. 30 ع. 18: 3151–3156. Bibcode:1996AtmEn..30.3151P. DOI:10.1016/1352-2310(96)00026-X. مؤرشف من الأصل في 2022-04-21.
- ^ Leman L، Orgel L، Ghadiri MR (2004). "Carbonyl sulfide-mediated prebiotic formation of peptides". Science. ج. 306 ع. 5694: 283–6. Bibcode:2004Sci...306..283L. DOI:10.1126/science.1102722. PMID:15472077.
| كبريتيد الكربونيل في المشاريع الشقيقة: | |